Hội chứng Lambert-Eaton là một rối loạn thần kinh – cơ hiếm gặp nhưng cực kỳ nghiêm trọng, có thể ảnh hưởng đến khả năng vận động và chất lượng sống của người bệnh. Bệnh thường bị nhầm lẫn với nhược cơ, dẫn đến chẩn đoán sai và điều trị chậm trễ. Hiểu rõ về hội chứng này là bước đầu tiên để kiểm soát hiệu quả và cải thiện tiên lượng bệnh.
Trong bài viết này, ThuVienBenh.com sẽ cung cấp cho bạn cái nhìn toàn diện nhất về hội chứng Lambert-Eaton: từ nguyên nhân, triệu chứng, đến các phương pháp chẩn đoán và điều trị hiện đại nhất.
Tổng quan về hội chứng Lambert-Eaton
Định nghĩa y học
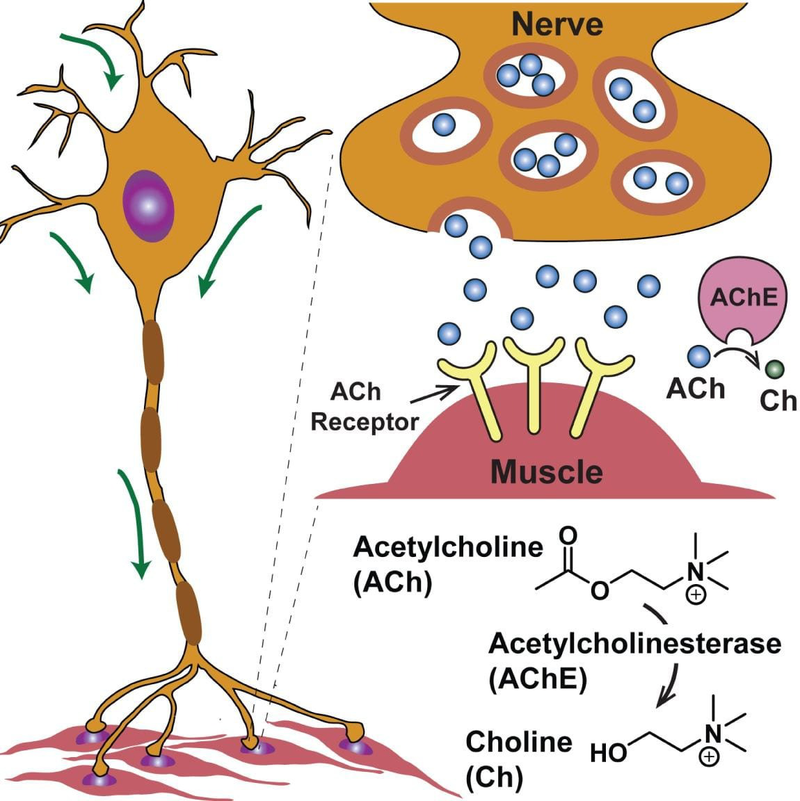
Hội chứng Lambert-Eaton (Lambert-Eaton Myasthenic Syndrome – LEMS) là một rối loạn tự miễn, trong đó hệ miễn dịch tấn công nhầm các kênh canxi điện thế ở đầu tận thần kinh, làm suy giảm giải phóng acetylcholine – chất trung gian truyền dẫn thần kinh đến cơ. Điều này dẫn đến yếu cơ dần tiến triển, đặc biệt ở chi dưới.
LEMS là bệnh lý hiếm gặp, với tỷ lệ mắc khoảng 1 trên 100.000 người, thường xuất hiện ở người trung niên và có liên quan mật thiết đến ung thư, đặc biệt là ung thư phổi tế bào nhỏ (SCLC).
Phân loại hội chứng Lambert-Eaton
- LEMS liên quan đến ung thư (Paraneoplastic LEMS): Chiếm khoảng 50–60% trường hợp, chủ yếu liên quan đến SCLC.
- LEMS không do ung thư (Idiopathic LEMS): Không tìm thấy nguyên nhân ung thư rõ ràng, thường có tiên lượng tốt hơn.
Nguyên nhân gây hội chứng Lambert-Eaton
Yếu tố tự miễn và sinh bệnh học
Cơ chế bệnh sinh chủ yếu của LEMS là rối loạn tự miễn. Cơ thể sản xuất kháng thể chống lại kênh canxi điện thế phụ thuộc điện (VGCC – voltage-gated calcium channel) tại đầu tận dây thần kinh vận động. Khi các kháng thể này ngăn cản VGCC hoạt động, quá trình phóng thích acetylcholine giảm sút, gây yếu cơ.
Khoảng 85–90% bệnh nhân LEMS có thể xét nghiệm dương tính với kháng thể anti-VGCC, là một chỉ dấu đặc hiệu quan trọng trong chẩn đoán.
Mối liên hệ với ung thư phổi tế bào nhỏ
Sự liên kết giữa LEMS và ung thư phổi tế bào nhỏ (SCLC) đã được ghi nhận rõ ràng trong y văn. Theo thống kê:
- Khoảng 50–60% bệnh nhân LEMS có SCLC.
- Trong số bệnh nhân SCLC, khoảng 3% sẽ phát triển hội chứng Lambert-Eaton như một biểu hiện cận u (paraneoplastic).
Các tế bào ung thư có thể biểu hiện các protein giống VGCC, kích thích hệ miễn dịch tạo ra kháng thể chống lại cả ung thư và kênh canxi ở thần kinh ngoại biên.
Triệu chứng và dấu hiệu lâm sàng
Yếu cơ và biểu hiện thần kinh
Triệu chứng đặc trưng nhất của LEMS là yếu cơ gốc chi, đặc biệt là cơ hông và đùi. Người bệnh thường gặp khó khăn khi:
- Leo cầu thang
- Đứng lên từ tư thế ngồi
- Đi bộ quãng dài
Một điểm quan trọng để phân biệt với nhược cơ là: cơ lực có thể cải thiện sau vận động (gọi là hiện tượng “facilitation”). Ví dụ, sau khi đứng lên – ngồi xuống vài lần, cơ lực có thể tăng rõ rệt trong thời gian ngắn.
So sánh với bệnh nhược cơ thông thường
| Đặc điểm | Hội chứng Lambert-Eaton | Bệnh nhược cơ (Myasthenia Gravis) |
|---|---|---|
| Vị trí yếu cơ | Chi dưới (gốc chi) | Vùng mắt, mặt, họng |
| Diễn tiến sau vận động | Cải thiện tạm thời | Yếu tăng dần |
| Kháng thể đặc hiệu | Anti-VGCC | Anti-AChR hoặc Anti-MuSK |
| Liên quan đến ung thư | Phổ biến (SCLC) | Hiếm gặp |
Biểu hiện toàn thân khác
LEMS có thể kèm theo các triệu chứng tự động như:
- Khô miệng
- Táo bón
- Rối loạn huyết áp tư thế
- Giảm tiết mồ hôi
Các triệu chứng này cho thấy sự ảnh hưởng không chỉ ở thần kinh vận động mà còn ở hệ thần kinh tự động.
Quá trình chẩn đoán
Khám lâm sàng và hỏi bệnh
Việc chẩn đoán bắt đầu từ khám lâm sàng kỹ càng và hỏi bệnh chi tiết. Bác sĩ sẽ lưu ý các dấu hiệu như:
- Yếu cơ đối xứng ở gốc chi
- Cải thiện cơ lực sau vận động
- Rối loạn thần kinh tự động
Xét nghiệm điện sinh lý và máu
Các công cụ chẩn đoán cận lâm sàng đóng vai trò rất quan trọng, bao gồm:
- Điện cơ (EMG): Tăng biên độ đáp ứng cơ sau kích thích lặp lại nhanh – là dấu hiệu kinh điển của LEMS.
- Xét nghiệm kháng thể: Anti-VGCC dương tính ở ~90% trường hợp.
Hình ảnh học và tầm soát ung thư
Do LEMS có mối liên hệ mật thiết với ung thư phổi, việc tầm soát là cần thiết:
- Chụp CT ngực độ phân giải cao
- Chụp PET/CT toàn thân nếu nghi ngờ di căn
Case study thực tế: Một bệnh nhân nữ 48 tuổi với dấu hiệu yếu chân
Chị H., 48 tuổi ở TP.HCM, nhập viện với biểu hiện yếu hai chân và khó đi lại. Ban đầu được chẩn đoán nhược cơ nhưng không đáp ứng điều trị. Sau khi làm điện cơ và xét nghiệm anti-VGCC, bác sĩ xác định chị mắc hội chứng Lambert-Eaton. Chụp CT cho thấy có khối u phổi nhỏ tế bào, được xử lý phẫu thuật kèm hóa trị. Hiện tại chị đã có thể vận động bình thường trở lại.
Các phương pháp điều trị hiện nay
Điều trị triệu chứng
Mục tiêu chính trong điều trị LEMS là cải thiện chức năng vận động và giảm triệu chứng yếu cơ. Các thuốc thường dùng bao gồm:
- 3,4-Diaminopyridine (3,4-DAP): Là thuốc đầu tay giúp tăng phóng thích acetylcholine ở đầu tận thần kinh, cải thiện cơ lực đáng kể.
- Amifampridine (Firdapse): Dạng cải tiến của 3,4-DAP, được FDA chấp thuận cho điều trị LEMS.
- Thuốc ức chế cholinesterase: Như pyridostigmine, hiệu quả thấp hơn nhưng có thể hỗ trợ khi phối hợp với các thuốc khác.
Điều trị nền tảng (tự miễn và ung thư)
Ở nhóm bệnh nhân có LEMS tự miễn thuần túy, các thuốc ức chế miễn dịch được chỉ định như:
- Prednisone (corticoid)
- Azathioprine hoặc Mycophenolate mofetil
- Rituximab – một kháng thể đơn dòng tiêu diệt tế bào B
Đối với LEMS cận ung thư (paraneoplastic), việc điều trị ung thư gốc (thường là ung thư phổi tế bào nhỏ) sẽ đồng thời cải thiện triệu chứng LEMS. Các phương pháp bao gồm:
- Phẫu thuật cắt bỏ khối u (nếu có thể)
- Hóa trị và xạ trị đồng thời
Vai trò của thuốc tăng dẫn truyền thần kinh
3,4-DAP là thuốc nền tảng trong kiểm soát triệu chứng LEMS. Một nghiên cứu năm 2020 trên tạp chí Neurology cho thấy:
- 80% bệnh nhân dùng 3,4-DAP có cải thiện cơ lực đáng kể sau 6 tuần.
- Tác dụng phụ thường nhẹ, bao gồm đau bụng, rối loạn giấc ngủ.
Hiệu quả của 3,4-DAP và Rituximab
Một nghiên cứu hồi cứu tại Pháp cho thấy nhóm bệnh nhân điều trị kết hợp 3,4-DAP và Rituximab đạt tỷ lệ cải thiện lâm sàng trên 60%, duy trì hiệu quả ít nhất 12 tháng.
Tiên lượng và biến chứng
Yếu tố tiên lượng tốt
Tiên lượng của hội chứng Lambert-Eaton phụ thuộc vào nguyên nhân nền và thời điểm điều trị:
- LEMS không liên quan ung thư thường có tiên lượng tốt, đáp ứng điều trị cao.
- Phát hiện và điều trị ung thư sớm giúp cải thiện rõ rệt triệu chứng thần kinh.
Biến chứng nguy hiểm nếu không điều trị
Nếu không được phát hiện và điều trị đúng cách, LEMS có thể dẫn đến:
- Liệt cơ hô hấp, nguy hiểm đến tính mạng
- Giảm khả năng vận động, phụ thuộc người chăm sóc
- Trầm cảm và giảm chất lượng sống
Hội chứng Lambert-Eaton khác với bệnh nhược cơ như thế nào?
So sánh về nguyên nhân
LEMS là bệnh tự miễn có liên quan đến kênh canxi ở đầu tận thần kinh, trong khi nhược cơ (Myasthenia Gravis) liên quan đến kháng thể chống thụ thể acetylcholine ở màng sau synapse.
So sánh về cơ chế sinh bệnh
- LEMS: Suy giảm giải phóng acetylcholine từ đầu tận thần kinh
- Nhược cơ: Acetylcholine không gắn được vào thụ thể ở cơ
Khác biệt trong đáp ứng với điều trị
LEMS đáp ứng tốt với 3,4-DAP và thuốc ức chế miễn dịch. Nhược cơ thường ưu tiên điều trị bằng pyridostigmine, corticoid, hoặc phẫu thuật tuyến ức.
Làm thế nào để sống khỏe với hội chứng Lambert-Eaton?
Chế độ dinh dưỡng và luyện tập
Người bệnh cần tuân thủ chế độ ăn uống cân bằng, nhiều protein và vitamin nhóm B. Nên duy trì luyện tập nhẹ nhàng để giữ sức cơ, tránh nằm lâu.
Theo dõi định kỳ và hỗ trợ tâm lý
- Thăm khám chuyên khoa thần kinh định kỳ mỗi 3–6 tháng.
- Tầm soát ung thư phổi định kỳ nếu chưa xác định nguyên nhân.
- Tham vấn tâm lý khi gặp khó khăn trong thích nghi với bệnh mạn tính.
Kết luận
Tầm quan trọng của phát hiện sớm
Hội chứng Lambert-Eaton là bệnh lý hiếm gặp nhưng có thể điều trị hiệu quả nếu được phát hiện sớm. Việc chẩn đoán đúng không chỉ giúp cải thiện vận động mà còn phát hiện các khối u tiềm ẩn nguy hiểm như ung thư phổi.
Trích dẫn một câu chuyện thực tế
“Tôi từng không thể đứng dậy nổi sau mỗi buổi sáng. Các bác sĩ nghĩ tôi bị nhược cơ, nhưng xét nghiệm sau đó xác nhận tôi mắc hội chứng Lambert-Eaton. Nhờ chẩn đoán đúng và điều trị sớm, tôi đã có thể quay lại công việc và sống khỏe mạnh hơn.” – Chị H. (48 tuổi, TP.HCM)
Câu hỏi thường gặp (FAQ)
1. Hội chứng Lambert-Eaton có chữa khỏi được không?
Không có phương pháp chữa khỏi hoàn toàn, nhưng điều trị đúng có thể giúp kiểm soát triệu chứng và cải thiện chất lượng sống đáng kể.
2. Có nên sàng lọc ung thư khi được chẩn đoán LEMS?
Có. Do mối liên hệ chặt chẽ với ung thư phổi tế bào nhỏ, người bệnh cần được chụp CT ngực và tầm soát định kỳ.
3. LEMS có di truyền không?
Không. Đây là bệnh tự miễn và không mang tính di truyền trong gia đình.
4. Có phải tất cả bệnh nhân LEMS đều cần dùng thuốc ức chế miễn dịch?
Không. Tùy thuộc vào nguyên nhân nền và mức độ nặng của bệnh. Một số trường hợp nhẹ có thể kiểm soát chỉ bằng thuốc tăng dẫn truyền thần kinh.
5. Hội chứng Lambert-Eaton có thể tái phát không?
Có thể, đặc biệt nếu nguyên nhân nền như ung thư không được kiểm soát triệt để. Do đó, việc theo dõi định kỳ là rất quan trọng.
📝Nguồn tài liệu: Chọn lọc từ nhiều nguồn y tế uy tín
🔎Lưu ý: Bài viết chỉ nhằm mục đích cung cấp thông tin tổng quan. Vui lòng tham khảo ý kiến của Bác sĩ, Dược sĩ hoặc chuyên gia y tế để nhận được hướng dẫn phù hợp với tình trạng sức khỏe của bạn.

